蛋白质基本单位-20种氨基酸及其参与的PTM修饰
氨基酸作为蛋白质的基本结构单元,通过肽键共价连接形成多肽链,进而折叠成具有特定三维空间结构的蛋白质。蛋白质作为生命活动的核心执行体,几乎参与了所有细胞过程,包括催化生化反应(酶)、结构支撑、信号转导、物质运输及免疫应答等。蛋白质的功能复杂性不仅源于其一级序列,更受到翻译后修饰 的精密调控。PTM是指在蛋白质生物合成后,通过共价添加化学基团(如磷酸基、乙酰基、糖链等)或进行结构修饰(如蛋白水解切割),从而动态地改变蛋白质的活性、定位、稳定性及与其他分子的相互作用。这些修饰具有高度的位点特异性,通常发生在特定氨基酸残基的侧链上。例如:
磷酸化 常发生于丝氨酸(Ser,S)、苏氨酸(Thr,T)、酪氨酸(Tyr,Y)。
乙酰化 常发生于赖氨酸(Lys,K)。
糖基化 常发生于天冬酰胺(Asp,D)、丝氨酸(Ser,S)、苏氨酸(Thr,T)。
泛素化 则用于靶向蛋白降解,主要发生在赖氨酸(Lys,K)。
1、 氨基酸结构与功能
(图1 氨基酸通用结构式)
蛋白质合成的基石:这是最基本的功能,20种标准氨基酸以特定序列通过肽键连接,构成了蛋白质的一级结构。
(图2 20中常见氨基酸识记)
决定蛋白质的三维结构:氨基酸侧链(R基)的化学性质(疏水、亲水、带电、大小等)驱动蛋白质折叠成特定的三维构象,这是其功能的基础。
提供功能活性位点:在酶或受体的活性中心,特定的氨基酸侧链直接参与催化反应、底物结合或信号转导。例如:丝氨酸蛋白酶中的“催化三联体”(组氨酸、天冬氨酸、丝氨酸)共同协作,水解肽键。
介导蛋白质相互作用:带电氨基酸和极性氨基酸可以参与形成氢键、盐桥,从而介导蛋白质与蛋白质、蛋白质与核酸或其他配体之间的特异性相互作用。
二、 从功能上看:潜力与实现
氨基酸提供化学功能的“工具箱”:
20种标准氨基酸的侧链(R基)提供了多样化的化学功能团,包括:
疏水基团:驱动蛋白质折叠,形成疏水核心。
亲水/带电基团:形成氢键、盐桥,参与催化,或使蛋白质溶于水。
反应性基团(如半胱氨酸的巯基、丝氨酸的羟基):直接参与酶的催化反应。
蛋白质是功能的最终执行者:
当氨基酸链折叠成特定的三维结构后,这些分散的“化学工具”被精确地安置在蛋白质的空间架构中,形成一个功能性的整体。
例如:在酶的活性中心,来自序列上不同位置的几个特定氨基酸(如天冬氨酸、组氨酸、丝氨酸)被“召集”到一起,形成一个可以高效催化特定化学反应的精巧微环境。
三、从动态调控上看:修饰与调节
正如我们之前讨论的,氨基酸残基可以被化学修饰(如磷酸化、糖基化、乙酰化等)。这些修饰就像是在“砖块”上贴上小标签,可以动态地改变“大厦”的功能:激活或抑制酶的活性。指导蛋白质去往细胞的特定位置。调节蛋白质与其他分子的相互作用。
四、20种氨基酸识记
表1 常见氨基酸识记表
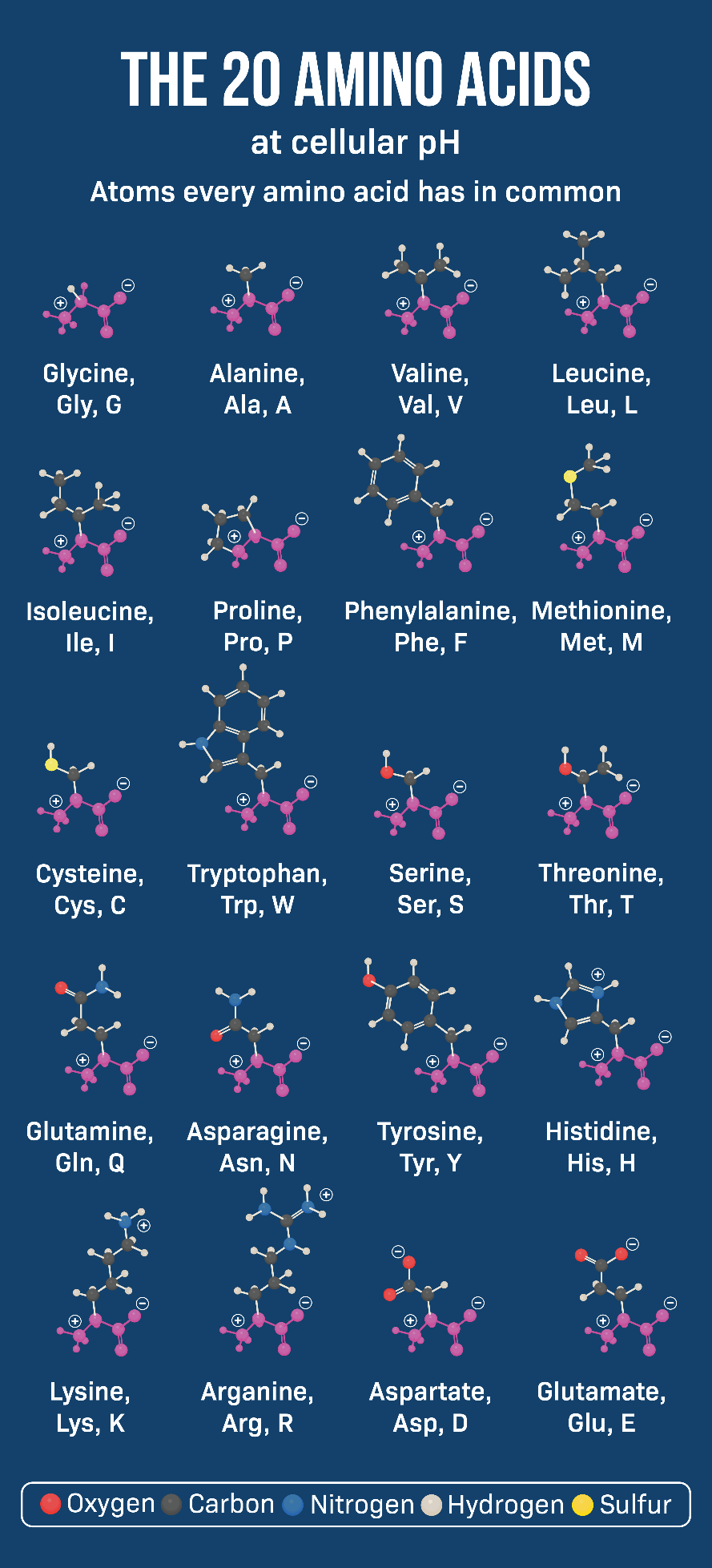
(图3 氨基酸识记表)
五、氨基酸修饰与蛋白功能
翻译后修饰 (PTM) 被认为是蛋白质功能微妙或显着改变的重要机制,并为细胞提供了调节不同分子过程的方法。PTM 调节蛋白质的折叠、定位、相互作用、降解和活性,它们基本上参与了所有生物过程。由于许多 PTM 的快速和可逆特性,它们也是信号传输的理想中介。
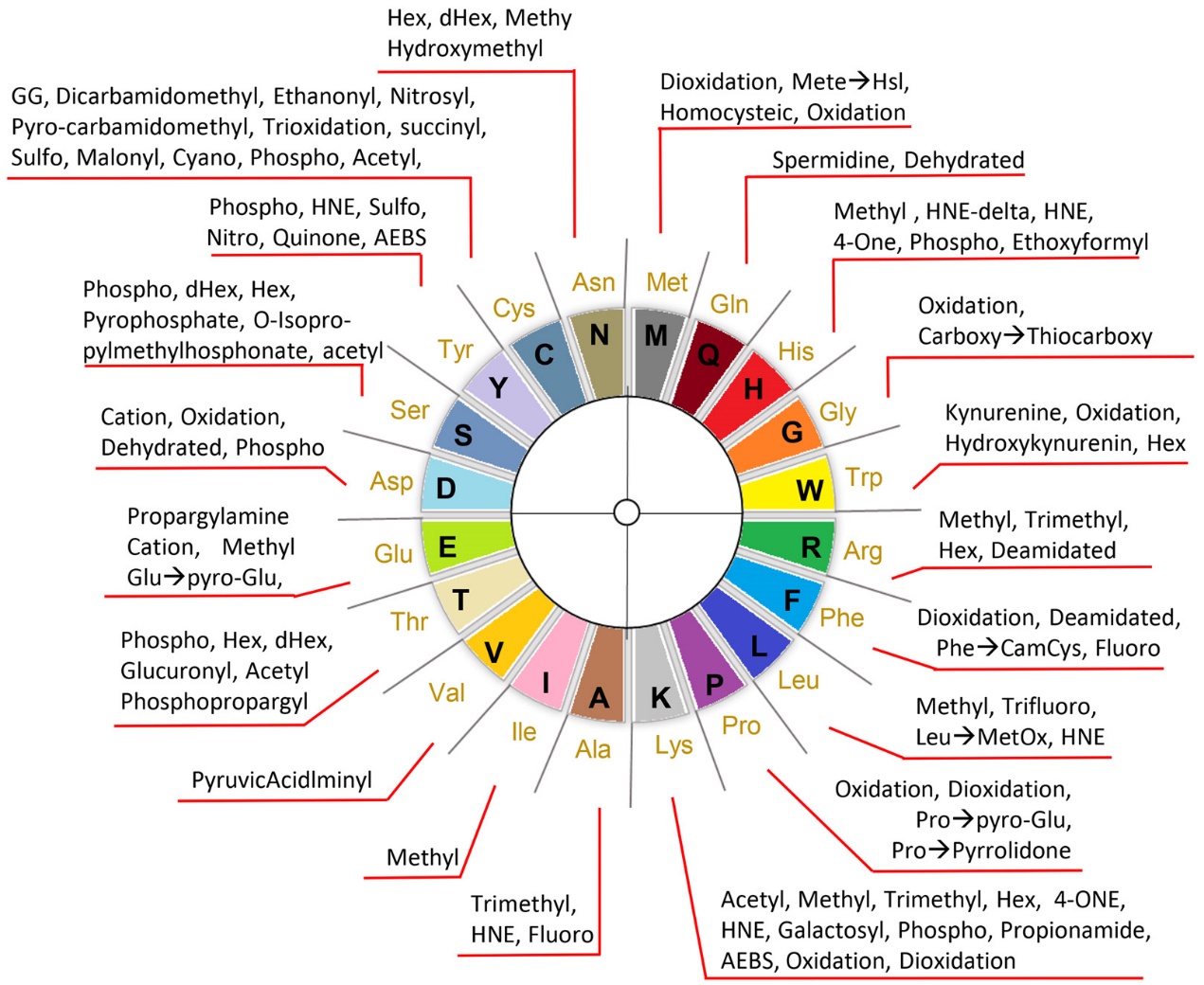
(图4 氨基酸涉及到的修饰类型[1])
表2 蛋白质翻译后修饰涉及到的氨基酸及其影响的主要功能
参考:
Bagwan N, El Ali HH, Lundby A. Proteome-wide profiling and mapping of post translational modifications in human hearts. Sci Rep. 2021 Jan 26;11(1):2184. doi: 10.1038/s41598-021-81986-y . PMID: 33500497; PMCID: PMC7838296.